Chemische Reaktivität
Many smell molecules exhibit chemical reactivity.
Viele Geruchsmoleküle weisen eine chemische Reaktivität auf. Dies ist zum Teil die Antwort darauf, warum ihr Geruch oft so intensiv ist – weil sie die Rezeptoren des Riechepithels stimulieren, was zu einer starken psychophysiologischen Reaktion führt. Aldehyde sind auch chemisch reaktiv, und es kann nachgewiesen werden, dass einige der Moleküle, die z. B. für „populäre“ schlechte Gerüche verantwortlich sind, mit ihnen reagieren und neue Moleküle mit deutlich reduziertem oder gar keinem Geruch bilden. Die chemische Reaktivität der Aldehydgruppe -CHO liegt zahlreichen Prozessen in der modernen chemischen Industrie zugrunde, vor allem bei der Herstellung von Harzen und Kunststoffen sowie von Hygiene- und Desinfektionsmitteln. Das einfachste Aldehyd, Formaldehyd HCHO, ist ein wichtiger Bestandteil von Melamin, Harnstoff und Acetalharzen. Es ist auch Bestandteil des ersten vollsynthetischen Kunststoffs – Bakelit, d.h. des Phenol-Formaldehyd-Harzes.

Außerdem ist Formaldehyd immer noch ein weit verbreitetes Desinfektions- und Begasungsmittel (ein Desinfektionsmittel, das Rauch erzeugt). Für unsere Zwecke ist Formaldehyd jedoch nutzlos. Es ist zu reaktiv, hat einen starken, stechenden und reizenden Geruch (wirkt auf die Trigeminusnervenenden) und ist ansonsten giftig. Es gibt jedoch viele andere Aldehyde, die bekannt sind und verwendet werden. Fast alle haben einen interessanten Duft und werden häufig zur Herstellung von aromatischen und aromatisierten Produkten verwendet. Wir haben entdeckt, dass einige Aldehyde stabile chemische Reaktionen mit einer breiten Palette von geruchsaktiven Verbindungen eingehen, aber auch mit anderen Geruchsverbindungen, die keine eindeutig negativen Assoziationen hervorrufen (z. B. Kaffeeduft). Dadurch haben wir ein neues Werkzeug im Kampf gegen belästigende Gerüche erhalten, dessen Anwendungsbereiche grenzenlos sind.
Unsere Neutralisatoren sind eine Mischung aus mindestens zwei Aldehydneutralisatoren, von denen einer eine ungesättigte Bindung am Kohlenstoff in der Alpha-Position der CHO-Gruppe aufweist und der andere nicht. Die Wirkstoffe der Präparate wirken durch nukleophile Additions- oder Substitutionsreaktionen mit Stickstoff und Schwefel am Kohlenstoff von ausgewählten Aldehyden und Ketonen. Die daraus resultierenden Reaktionen sind irreversibel. Diese Idee wurde weiterentwickelt, als sich herausstellte, dass bestimmte Aldehydpaare bei der Bindung von Gerüchen zusammen wirksamer sind, als wenn sie einzeln reagieren würden. Infolge dieser Entdeckung fanden wir weitere derartige Reaktionen mit mindestens 2 und mehr Kombinationen von Aldehyden, Ketonen und Ketoalkinen.

In vielen Fällen wurde der Mechanismus der Reaktion nicht vollständig verstanden und beschrieben. Empirisch können wir nachweisen, dass solche Paare wirken und die Wirksamkeit des Neutralisationsgemisches bei der Verringerung der Konzentration unerwünschter Stoffe in der Luft erhöhen.
Bei der neuesten Generation von Neutralisatoren haben wir es auch mit der Additionsreaktion (Anlagerungsreaktion) zu tun, bei der die Kohlenstoff-Kohlenstoff-Mehrfachbindung aufgebrochen wird. Im Allgemeinen sind diese Reaktionen weder schnell noch zu 100% abgeschlossen, bis die neutralisierenden Bestandteile in ausreichendem Überschuss auftreten, um die Reaktionen zum Abschluss zu bringen.
Nachfolgend sind Beispiele für ausgewählte Reaktionen von Aldehyden mit Geruchsstoffen aufgeführt, die eine Thiol- und eine Amingruppe enthalten.
Beispiel für die Reaktion eines Aldehyds mit einem einfachen primären Amin:
RCHO + R1NH2 → RCH = NR1 + H2O
Beispiel für die Reaktion eines Aldehyds mit Mercaptan:
R1CHO + 2R2SH → R1CH(SR)2 + H2O
In beiden Fällen sind die resultierenden Moleküle im Allgemeinen weniger flüchtig, und die osmophoren Atome von Stickstoff (N) oder Schwefel (S) sind im Molekül praktisch „versteckt” und haben nicht mehr die gleiche Kraft, die Geruchsrezeptoren zu reizen.
Bei komplexeren Diaminen wie Putrescin gibt es zwei Aminogruppen, die ebenfalls mit dem Aldehyd reagieren:
↑H2NCH2CH2CH2CH2NH2↑
Diese besonders unangenehmen Stoffe haben also eine doppelte „Chance”, neutralisiert zu werden. Die dargestellten Gleichungen dienen nur zur Veranschaulichung.
Wenn wir also davon ausgehen, dass es beim Zusammentreffen der Moleküle der beiden Stoffe zu einer chemischen Reaktion kommt, wie oben beschrieben, und beide Verbindungen in der Mindestkonzentration auftreten, die sie wahrnehmbar macht, dann lautet eines der chemischen Grundgesetze, dass diese Reaktion von dem Stoff, der im Überschuss vorhanden ist, so lange „angetrieben“ wird, bis (fast) kein Molekül des unangenehmen Geruches mehr übrig ist.
Diese Reaktionen laufen je nach Art der zu neutralisierenden Verbindung unterschiedlich schnell ab. In seltenen Fällen können diese Reaktionen unvollständig sein, so dass mehr Zeit und ein gewisser Überschuss des Präparats erforderlich sind. Der pH-Wert der Umgebung hat einen großen Einfluss auf die Kinetik der Reaktion. Wenn wir also die Desodorierung von Abwasser betrachten, werden die besten Ergebnisse außerhalb der pH-Extremwerte erzielt.
Chemische Reaktionen
Ammoniak, Amine und Schwefelwasserstoff sind unter den zahlreichen Geruchsgruppen die am häufigsten
Ammoniak, Amine und Schwefelwasserstoff sind unter den zahlreichen Geruchsgruppen die am häufigsten vorkommenden Luftschadstoffe.
Die Wirkstoffe der WESTRAND-Präparate wirken durch nukleophile Reaktionen mit Stickstoff und Schwefel am d+ Kohlenstoff der C=O-Gruppe von Aldehyden und Ketonen. Im Allgemeinen sind diese Reaktionen weder schnell noch zu 100% abgeschlossen, bis die neutralisierenden Bestandteile in ausreichendem Überschuss auftreten, um die Reaktionen zum Abschluss zu bringen. Die Kinetik dieser Reaktionen wird durch den pH-Wert der Reaktionsumgebung und die Temperatur beeinflusst.
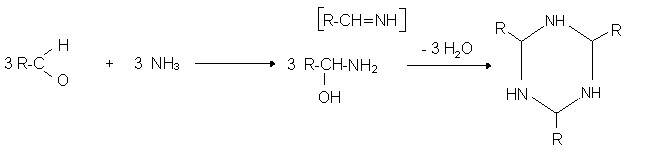
RReaktionen eines Aldehyds mit Ammoniak:
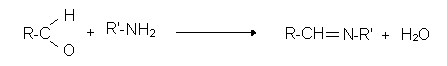
Reaktionen eines Aldehyds mit Aminen:
- primäre Amine
- sekundäre Amine
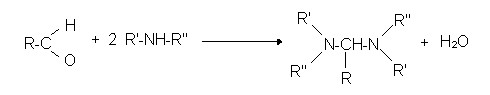
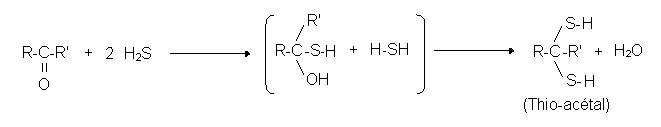
Reaktionen eines Aldehyds mit Mercaptanen:
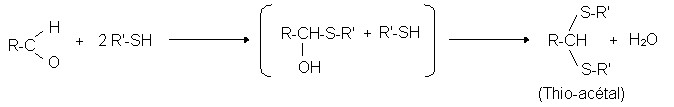
- H2S
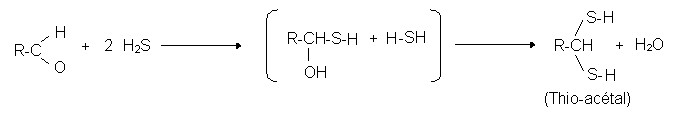
Reaktionen von Ketonen mit Ammoniak:
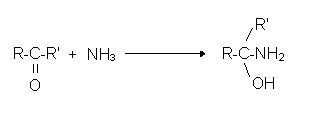
Reaktionen von Ketonen mit Aminen:
- primäre Amine
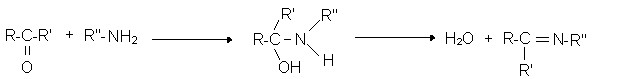
(Imine oder Schiff’sche Base)
- sekundäre Amine
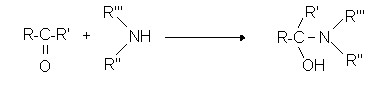
Reaktionen von Ketonen mit Mercaptanen:
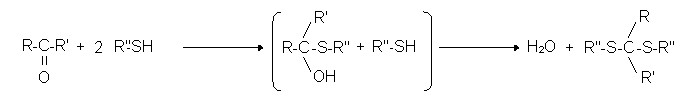
- H2S